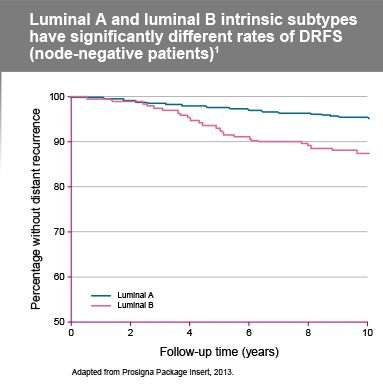
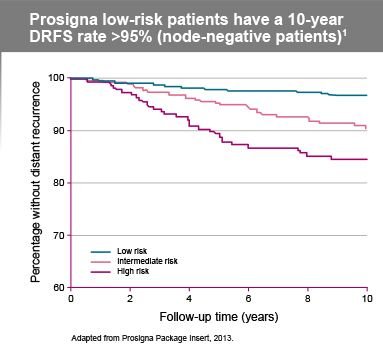
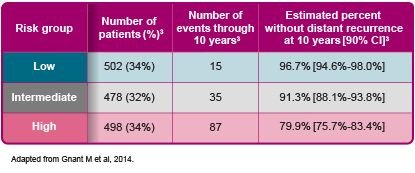
Prosigna, birden fazla alan ve operatör arasında yüksek düzeyde uyumlu sonuçlar sağlar1,2
Prosigna'nın analitik doğrulama çalışması, birden fazla kalifiye laboratuvarda yüksek hassasiyet ve tekrarlanabilirlik gösterdi2
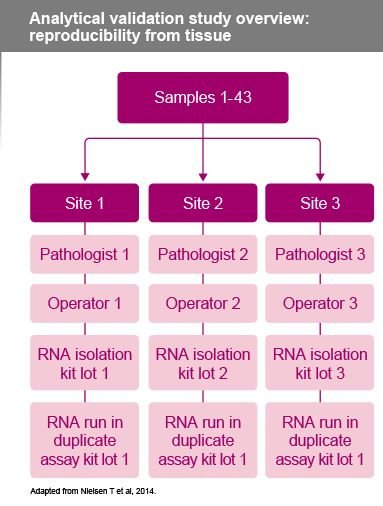
Amaç: Nitelikli klinik laboratuvarlarda kullanıldığında Prosigna'nın analitik sağlamlığının 2 yönünü değerlendirin: dokudan başlarken tekrarlanabilirlik ve RNA'dan başlarken kesinlik
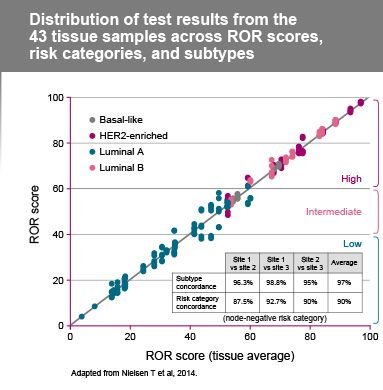
Dokudan başlayarak, toplam standart sapma 3 bağımsız bölgede sadece 2.9 Nüksetme Riski (ROR) Birimiydi
- Tekrarlanabilirlik, bağımsız H&E incelemesi, makrodiseksiyon ve her bir sahadaki laboratuvar personeli tarafından RNA izolasyonu dahil olmak üzere 3 sahada 43 FFPE bloğundan oluşan bir panel test edilerek değerlendirildi.
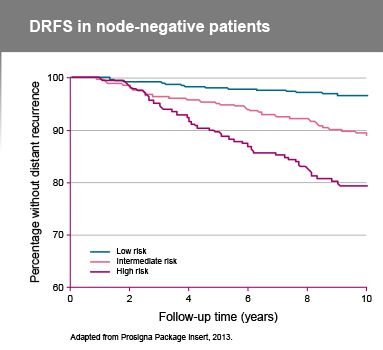
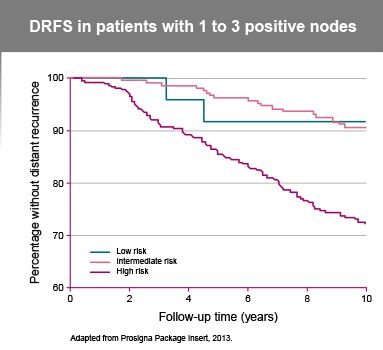
- Risk kategorisinin ortalama site-to-site uyumu>%90'dı ve düşük ila yüksek riskli yanlış sınıflandırmalar ya da tam tersi yoktu.
- Alt tür sınıflandırmasının ortalama siteden siteye uyumu %97 idi.
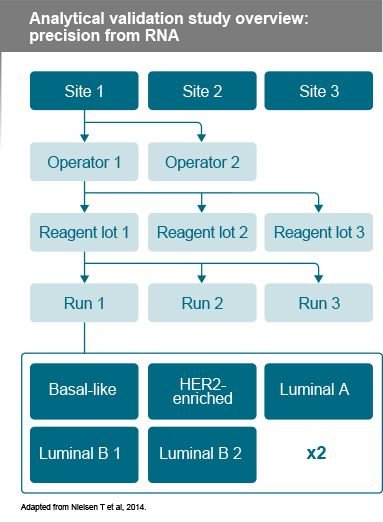
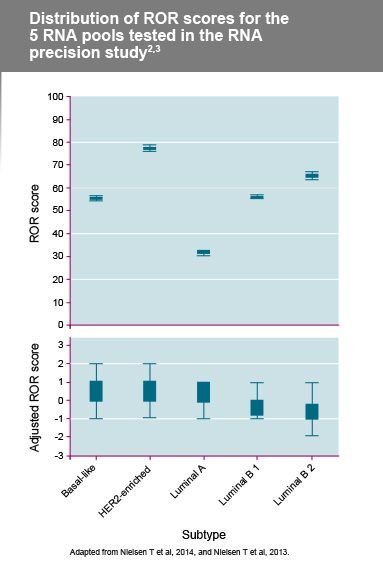
RNA'dan başlayarak, test yeri, operatör ve reaktif lotundan bağımsız olarak toplam standart sapma <1 ROR birimiydi
- Kesinlik, 5 havuzlanmış FFPE meme tümörü RNA numunesinin her biri >100 kez test edilmesiyle değerlendirildi.
- RNA örnekleri, 3 farklı reaktif lotu kullanılarak toplam 6 farklı operatör tarafından 3 farklı test sahasında bağımsız olarak çalıştırıldı.
- 108 bağımsız ölçüm için ROR skorları aralığı, 5 örnek havuzunun her biri için ≤4 birimdir.
- Ölçülen ve beklenen alt tip sonucu ile risk grubu arasında 0 uyum gösterildi.
References: 1. Prosigna [Package Insert]. Seattle, WA: NanoString Technologies, Inc; 2013. 2. Nielsen T, Wallden B, Schaper C, et al. Analytical validation of the PAM50-based Prosigna Breast Cancer Prognostic Gene Signature Assay and nCounter Analysis System using formalin-fixed paraffin-embedded breast tumor specimens [published online ahead of print March 13, 2014]. BMC Cancer. doi:10.1186/1471-2407-14-177. 3. Nielsen T, McDonald S, Kulkarni S, et al. Analytical reproducibility of the breast cancer intrinsic subtyping test and nCounter® Analysis System using formalin-fixed paraffin-embedded (FFPE) breast tumor specimens. Poster presented at: 102nd United States and Canadian Academy of Pathology Annual Meeting; March 2-8, 2013; Baltimore, MD. Abstract 2075.